Fontes de energia para a contração do músculo esquelético
A fibra muscular esquelética é adaptada para a produção de trabalho mecânico intenso e descontínuo, necessitando de depósitos de compostos ricos em energia. A energia que pode ser mobilizada com mais facilidade é a acumulada em ATP e fosfocreatina ou creatina fosfato (CP), ambos compostos ricos em energia nas ligações fosfato e armazenados na célula muscular. Existe também energia nos depósitos sarcoplasmáticos de glicogênio.
Enquanto o músculo contrai, o ATP fornece a energia necessária para o movimento e o desligamento das pontes cruzadas e para a atividade da bomba de cálcio. Porém, o músculo armazena reservas muito limitadas de ATP — o suficiente para no máximo 4 a 6 segundos de atividade contrátil.
Como o ATP é a única fonte de energia usada diretamente para a atividade contrátil, ele deve ser regenerado tão rapidamente quanto é utilizado, caso a contração continue. Convenientemente, depois que o ATP é hidrolisado a ADP e fosfato inorgânico (Pi), ele é regenerado dentro de uma fração de segundo por três vias:
- pela interação do ADP com a fosfocreatina (CP): metabolismo anaeróbio alático (sem ácido lático) ou ATP-CP (fosforilação direta; não necessita de oxigênio para ocorrer);
- pela via anaeróbia (glicólise), que utiliza o glicogênio armazenado: metabolismo anaeróbio lático ou glicólise anaeróbia;
- pela respiração aeróbia: metabolismo aeróbio ou via aeróbia.
A taxa de conversão da energia química para mecânica durante a contração muscular é considerada um dos principais eventos fisiológicos determinantes do desempenho esportivo. Quando exercícios vigorosos são iniciados, a demanda de ATP aumenta e o ATP armazenado nos músculos ativos é consumido em poucas contrações musculares.
Então, a fosfocreatina (CP), uma molécula de alta energia exclusiva das células musculares, é usada para regenerar o ATP, enquanto as vias metabólicas estão se ajustando ao aumento súbito da demanda de ATP. O resultado do acoplamento da CP com o ADP é a transferência quase instantânea de energia e um grupo fosfato da CP para o ADP para a formação de ATP:
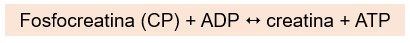
As células musculares armazenam 4 a 5 vezes mais CP do que ATP, e a reação CP-ADP, catalisada pela enzima creatina quinase (CK), é tão eficiente que a quantidade de ATP nas células musculares muda pouco durante o período inicial da contração. A reação acoplada é rapidamente reversível, e para manter os níveis de CP disponíveis, suas reservas são restabelecidas durante os períodos de inatividade.
Entretanto, a quantidade total de CP na fibra muscular é também muito pequena — apenas 4 a 5 vezes maior que a quantidade de ATP. Por isso, a energia combinada do ATP armazenado e da CP no músculo é capaz de manter a contração muscular máxima por apenas 5 a 8 segundos. Assim, enquanto o ATP armazenado e o CP são usados, mais ATP é gerado pelo catabolismo da glicose, obtida a partir da corrente sanguínea ou pela degradação do glicogênio armazenado no músculo. A fase inicial do metabolismo da glicose é a glicólise. Como esta via não usa oxigênio, ela é uma via anaeróbia (sem oxigênio).
Durante a glicólise, a glicose é parcialmente degradada no sarcoplasma em duas moléculas de piruvato, liberando energia suficiente para formar pequenas quantidades de ATP (2 ATPs por molécula de glicose).
OBS.:
A glicólise anaeróbia é o processo pelo qual uma sequência de aproximadamente 11 enzimas do citosol promovem degradação gradual em uma molécula de glicose, sem consumo de oxigênio, produzindo duas moléculas de piruvato e liberando energia que é armazenada em duas moléculas de ATP.

O ATP se forma a partir do ADP e do fosfato inorgânico (Pi) existentes no citosol, segundo a equação:

Essa degradação da glicose não necessita de oxigénio, razão pela qual é chamada de glicólise anaeróbia.
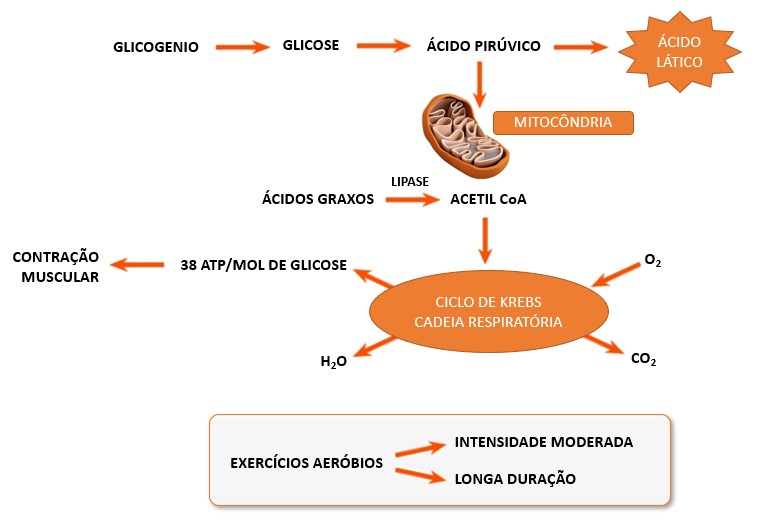
Geralmente o piruvato produzido na glicólise entra na mitocôndria e reage com o oxigênio para produzir muito mais ATP pela respiração aeróbia, via que utiliza oxigênio (via aeróbia ou metabolismo aeróbio). Durante a respiração aeróbia, que inclui a glicólise e as reações que ocorrem na mitocôndria (ciclo de Krebs e cadeia respiratória), a glicose é totalmente degradada, formando água, dióxido de carbono (CO2) e grandes quantidades de ATP (cerca de 38 ATPs por molécula de glicose) como produtos finais:
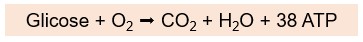

Entretanto, em exercícios de alta intensidade e duração relativamente curta, de 30 a 90 segundos, como, por exemplo, em corridas de 400 metros, quando os músculos contraem vigorosamente e a atividade contrátil alcança cerca de 70% da máxima, os músculos em contração comprimem os vasos sanguíneos dentro deles, prejudicando o fluxo sanguíneo e, portanto, o fornecimento de oxigênio. Sob essas condições anaeróbicas, a maioria do piruvato produzido durante a glicólise é convertida em ácido lático ou lactato, e todo o processo é referido como metabolismo anaeróbio lático ou glicólise anaeróbia.

O rápido desdobramento enzimático do glicogênio a ácidos pirúvico e lático libera energia que é utilizada para converter o ADP em ATP; o ATP pode então ser utilizado diretamente para energizar contrações musculares adicionais e também para reconstituir as reservas de CP.
Com o prolongamento da sessão de esforço, a participação do metabolismo aeróbio torna-se mais pronunciada, não excluindo a contribuição da via anaeróbia no fornecimento energético.
Assim, podemos criar uma ordem hierárquica de solicitação energética:
1- Metabolismo anaeróbio alático (sem ácido lático) ou ATP-CP: nos momentos iniciais, devido ao aumento abrupto da necessidade energética, a ativação da via anaeróbia tem grande participação no fornecimento energético, em função do déficit inicial de oxigênio. Nesta fase inicial de transição, a fosfocreatina (CP) é a principal responsável pelo desempenho do trabalho muscular durante o exercício, principalmente nos segundos iniciais, sendo sua demanda regulada pela atividade da enzima creatina quinase (CK). Este sistema é característico de exercícios de alta intensidade e curta duração, ou seja, atividades cuja duração fique em torno de seis a dez segundos, como exemplo a prova dos 100 m rasos no atletismo.
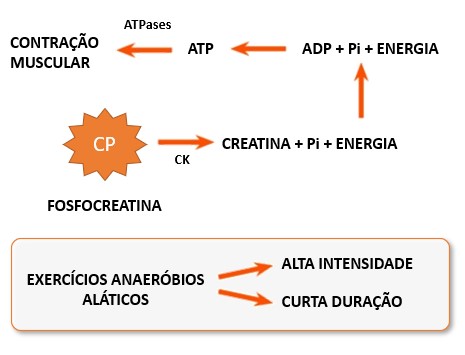
2- Metabolismo anaeróbio lático: é a segunda fonte importante de energia, que é utilizada para reconstituir o ATP e a CP. Caracteriza-se pelo processo no qual a glicose utilizada (proveniente da quebra do glicogênio armazenado) é parcialmente degradada no citoplasma da célula muscular até ácido lático (lactato), que se acumula no local. O lactato produzido no músculo vai para a corrente sanguínea e daí para o fígado, onde é removido do sangue e metabolizado.
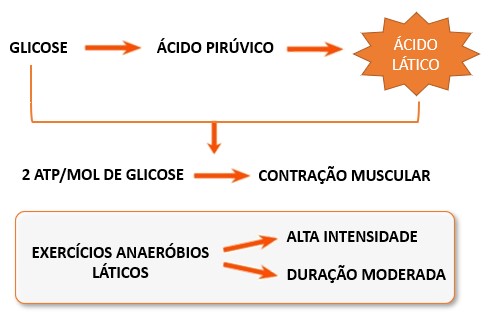
3- Metabolismo aeróbio: A energia liberada, pelos metabolismos anaeróbios alático e lático é rápida, porém relativamente pouco ATP é ressintetizado por estes mecanismos. Portanto temos a terceira via para a ressíntese de ATP, o metabolismo aeróbio, que ocorre na matriz mitocondrial (ciclo de Krebs) e nas cristas mitocondriais (cadeia respiratória) da mitocôndria.
OBS.:
No exercício moderado, da ordem de 65% do VO2max (consumo máximo de oxigênio ou capacidade máxima do organismo captar, transportar e utilizar o oxigênio), à medida em que ocorre o aumento da produção aeróbia de ATP, a síntese do ATP a partir do sistema ATP-CP diminui. Isso significa que um indivíduo que realiza um exercício em fase estável que se sustenta às custas do metabolismo aeróbio, não irá, ao longo do exercício, decrescer sua concentração de CP. Ele terá até uma reserva, devido à quantidade de CP mantida após o sistema metabólico energético assumir a demanda energética.
Classificação das fibras musculares esqueléticas
De acordo com sua estrutura e composição molecular, as fibras musculares esqueléticas podem ser classificadas como:
- tipo I: fibras de contração lenta ou fibras vermelhas,
- tipo II: fibras de contração rápida ou fibras brancas.
Quando um músculo é ativado ele desenvolve tensão (contrai). As fibras do tipo I (contração lenta) demoram mais para desenvolver o pico de tensão (≈80 milissegundos ou 80 ms ou 80 mseg) após sua ativação do que as fibras do tipo II (contração rápida) (≈30 mseg).
As diferenças bioquímicas entre os dois tipos básicos de fibra focam principalmente em sua capacidade de atividades oxidativas (respiração aeróbia ou metabolismo aeróbio) e glicolíticas (glicólise anaeróbia ou metabolismo anaeróbio lático). As fibras do tipo I, especialmente ricas em mioglobina, são classificadas como fibras vermelhas, enquanto as fibras do tipo II, que contêm consideravelmente menos mioglobina, são classificadas como fibras brancas. As fibras de contração lenta do tipo I tendem a ter níveis significativamente mais elevados de enzimas oxidativas do que as fibras de contração rápida do tipo II, que normalmente têm uma alta atividade glicolítica.
As propriedades contráteis lentas das fibras do tipo I parecem resultar em grande parte de:
- atividade relativamente baixa da miosina ATPase na miofibrila;
- capacidade de manipular o Ca2+ mais lenta: taxa mais lenta de liberação e captação de Ca2+ pelo retículo sarcoplasmático;
- velocidade de encurtamento do sarcômero (contração) mais lenta;
- mitocôndrias grandes e numerosas e, consequentemente, níveis significativamente mais elevados de enzimas oxidativas;
- capacidade glicolítica menos bem desenvolvida que as fibras de contração rápida.
Essas propriedades parecem conferir uma resistência relativamente alta à fadiga nas fibras do tipo I.
Já as fibras do tipo II (contração rápida) exibem:
- alta capacidade para transmissão dos potenciais de ação;
- alta atividade da miosina ATPase;
- liberação e captação rápidas de Ca2+ por um retículo sarcoplasmático eficiente;
- alta taxa de renovação (turnover) das pontes cruzadas;
- capacidade glicolítica bem desenvolvida.
As fibras de contração rápida são mais ativadas em atividades rápidas e de curta duração e durante contrações musculares vigorosas, que dependem da participação predominante do metabolismo anaeróbio para a produção de energia.
As fibras do tipo II (contração rápida) são ainda subdivididas em dois tipos:
- IIA: considerada intermediária, por possuir algumas características da fibra lenta (maior potencial oxidativo e menor potencial glicolítico em comparação com as fibras do tipo IIB),
- IIB: também denominada tipo IIx, é considerada a fibra verdadeiramente rápida ou glicolítica.
Considerando as diferenças bioquímicas abordadas entre os dois tipos básicos, podemos considerar três tipos de fibras musculares primárias nos seres humanos:
- tipo I: contração lenta oxidativa,
- tipo IIA: contração rápida oxidativa,
- tipo IIB ou IIx: contração rápida glicolítica.

Os maratonistas (corredores de longas distâncias) possuem maior percentual de fibras do tipo I, pois em corridas de longas distâncias a alta densidade de mitocôndrias e o metabolismo aeróbico são os requisitos mais importantes. Já para os velocistas (corredores de curtas distâncias; ex.: 100 metros rasos) as fibras do tipo II, de contração rápida e metabolismo anaeróbico, são as mais frequentes.
Fadiga muscular
A fadiga muscular é a incapacidade do músculo esquelético gerar níveis elevados de força muscular ou manter esses níveis no tempo. Ou seja, é um estado de incapacidade fisiológica para a contração, mesmo que o músculo ainda possa estar recebendo estímulos e depende de:
- tipo, duração e intensidade do exercício;
- tipologia das fibras musculares recrutadas;
- nível de treino;
- condições ambientais de realização do exercício.
O termo fadiga tem sido associado a inúmeras manifestações de incapacidade funcional, evidenciadas durante e/ou após o exercício (máximo ou submáximo), tais como:
- declínio da força muscular;
- incapacidade de manter uma determinada intensidade de exercício no tempo;
- diminuição da velocidade de contração muscular;
- aumento do tempo de relaxamento muscular;
- variação das concentrações intra e extracelulares de alguns metabólitos e íons.
A fadiga muscular pode resultar de alterações da homeostasia no próprio músculo esquelético, ou seja, o resultado do decréscimo da força contrátil independentemente da velocidade de condução do impulso neural, habitualmente designada de fadiga com origem predominantemente periférica. Pode também ser o resultado de alterações na condução do impulso nervoso que chega ao músculo, traduzida por uma redução progressiva da velocidade e frequência de condução do impulso voluntário durante o exercício, normalmente denominada de fadiga com origem predominantemente central.
Porém, embora diversos fatores pareçam contribuir para a fadiga, suas causas específicas não são compreendidas completamente. Muitas evidências experimentais indicam que a fadiga ocorre devido a um problema no acoplamento excitação-contração ou no interior das próprias fibras musculares. Assim, a fadiga fisiológica é um mecanismo periférico mais do que um mecanismo central.
Para maiores informações, consulte:
- ASCENSÃO, A.; MAGALHÃES, J.; OLIVEIRA, J.; DUARTE, J.; SOARES, J. Fisiologia da fadiga muscular. Delimitação conceptual, modelos de estudo e mecanismos de fadiga de origem central e periférica. Revista Portuguesa de Ciências do Desporto 3(1): 108-123, 2003.
- KRONBAUER, G.A.; CASTRO, F.A.S. Estruturas elásticas e fadiga muscular. Rev Bras Ciênc Esporte 2013; 35(2): 503-520.
- MARQUES JUNIOR, N.K. Mecanismos fisiológicos da Fadiga. Revista Brasileira de Prescrição e Fisiologia do Exercício (RBPFEX) 2015; 9(56): 671-720.
- SANTOS, A.B.; BONA, R.L.; CASTRO, F.A.S.; TARTARUGA; L.A.P. Aspectos biomecânicos e fisiológicos da fadiga na locomoção humana: conceitos, mecanismos e aplicações. Revista Ciência em Movimento 2010; 23: 89-98.
- SANTOS, E.; HERRERA, J.B. Fisiologia da fadiga muscular: quebrando paradigmas. Educação Física em Revista 2009; 3(3).
Exercícios físicos e estresse oxidativo
Embora o treinamento físico induza adaptações benéficas, a realização de exercícios intensos ou prolongados, acima da intensidade habitual de esforço ou com frequência de treinamento muito elevada, suplanta a capacidade do sistema antioxidante endógeno e geralmente resulta em lesão oxidativa. Esta sobrecarga oxidativa, apesar de se fazer sentir mais intensamente nos músculos esqueléticos, tem sido relatada também em muitos outros órgãos e sistemas corporais responsáveis pela regulação e manutenção da homeostase, incluindo coração, rins, pulmões e sistemas imune e ósteo-articular.
A lesão muscular induzida pela realização de uma sessão de exercícios excêntricos pode ser decorrente da ruptura de tecidos conectivos ligados a miofibrilas adjacentes, da própria célula muscular, da lâmina basal adjacente à membrana plasmática, da membrana plasmática da célula muscular, do sarcômero, do retículo sarcoplasmático, ou ainda de uma combinação desses componentes.
Em humanos, por razões éticas e logísticas, as evidências de estresse e lesão oxidativos induzidos pelo exercício agudo têm sido essencialmente estudadas em nível sanguíneo, quer no plasma, quer nas células circulantes. Neste contexto, o aumento da concentração de proteínas citosólicas na circulação após o exercício reflete a lesão muscular.
As proteínas avaliadas frequentemente são a creatina quinase (CK), a lactato desidrogenase (LDH), a transaminase glutâmico-oxalacética (TGO – também chamada de aspartato aminotransferase ou AST) e a mioglobina, que, normalmente, são incapazes de atravessar a membrana plasmática. A presença dessas proteínas na circulação sanguínea reflete significativa alteração na estrutura e permeabilidade da membrana miofibrilar. Dentre elas, a CK é frequentemente descrita como melhor marcador indireto de dano muscular, sobretudo após o exercício de força ou outros exercícios que exijam ações predominantemente excêntricas.
O fenômeno de isquemia/reperfusão, que pode ocorrer durante o exercício físico ou após trauma, também é um importante fator no processo de produção de espécies reativas de oxigênio (ERO). Períodos de exercício intenso podem aumentar o estresse oxidativo devido à hipóxia (baixa concentração de oxigênio) e à reoxigenação temporárias que ocorrem no músculo exercitado, em função das contrações e relaxamentos estabelecidos ciclicamente. Durante a contração, a compressão vascular estabelece um quadro de isquemia e, portanto, de hipóxia; no relaxamento ocorre a reperfusão e, consequentemente, a reoxigenação. Uma vez que durante o exercício a circulação sanguínea é desviada para os músculos em atividade, outros tecidos também podem sofrer hipóxia temporária. Como consequência, esses tecidos recebem uma grande quantidade de oxigênio após o exercício, favorecendo a geração de ERO.
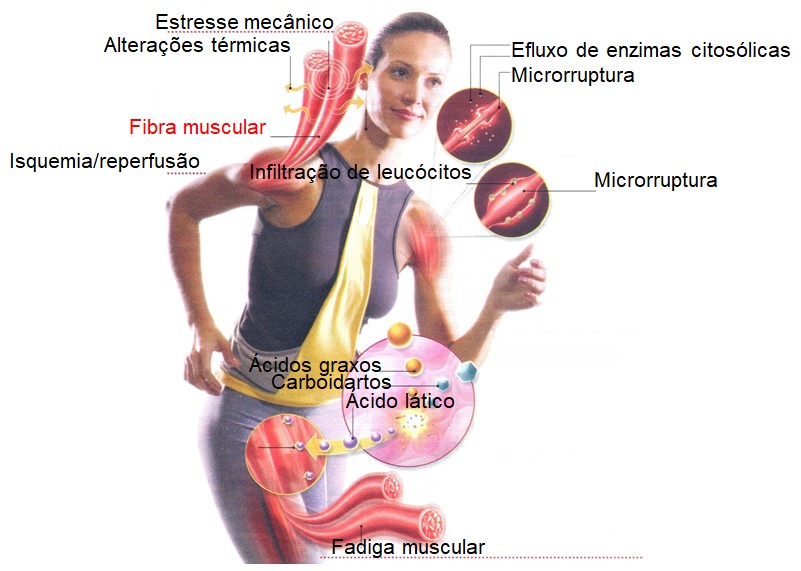
Para maiores informações, consulte:
- CRUZAT, V.F.; ROGERO, M.M.; BORGES, M.C.; TIRAPEGUI, J. Aspectos atuais sobre estresse oxidativo, exercícios físicos e suplementação. Rev Bras Med Esp 2007; 13(5): 336-342.
- FERREIRA F.; FERREIRA, R.; DUARTE, J. A. Stress oxidativo e dano oxidativo muscular esquelético: influência do exercício agudo inabitual e do treino físico. Rev Port Cien Desp 2007; 7(2) 257-275.
- MIRANDA-VILELA, A.L. Avaliação dos efeitos antigenotóxicos, antioxidantes e farmacológicos de extratos da polpa do fruto do pequi (Caryocar brasiliense CAMB). Tese (Doutorado em Biologia Animal). Universidade de Brasília, Brasília, 2009.
- PEDROSO, C.O.; KELI VICENZI, K.; ZANETTE, C. Efeitos do estresse oxidativo e o uso de suplementação entre atletas. Revista Brasileira de Nutrição Esportiva (RBNE) 2015; 9(53): 480-490.
Veja também:
- Saiba o que é cãibra e o que causa a lesão sofrida por brasileira no Pan.
- Malhar em jejum e mais: os erros na academia que todo iniciante comete.
